序にかえて
イノベーションにより加速する抗体医薬
津本浩平
(東京大学大学院工学系研究科バイオエンジニアリング専攻)
はじめに
がん,自己免疫疾患のような,いわゆるアンメットと言われた疾患領域で顕著な成果を上げてきた抗体医薬は,昨今のコロナパンデミックで,カクテル抗体という形で,広く一般に知られるようになった.長く抗体医薬開発研究の一端にいる筆者自身も,最近では,抗体が,タンパク質であり免疫系でつくられる重要な分子である,という説明をすることはあっても,抗体って何ですか,とか,なぜその研究をされているのですか,という問いへの返答に窮することは全くなくなった.今や児童も知っているPCRと同じように,いよいよ,抗体医薬は誰もが知るようになった,ということであろう.
国立医薬品食品衛生研究所の生物薬品部のホームページ1)に,医薬品として許認可されている抗体とその誘導体,類似体のリストがまとめられており,常に更新されている.以前はそれほど多くないとされていた標的,疾患も,今やきわめて多様性に富むものになっており,創薬モダリティとしての抗体は,バイオ医薬品の先頭走者として,ますますその活躍の場を増やしていることがよくわかる.
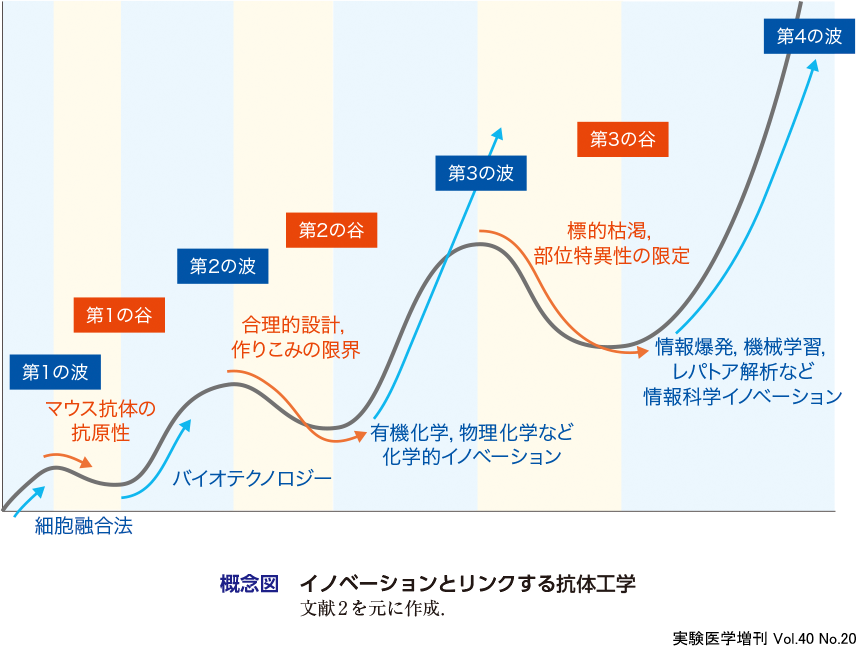
筆者は,実験医学2018年7月号で,抗体医薬特集を取りまとめるという大役を仰せつかり,当時,主に政府系プロジェクトにおいて最前線に立っておられる先生方を中心に御執筆いただいた2).幸い,当該号はたいへんな好評を博した.そのなかで,筆者は,イノベーションが抗体医薬の発展と密接に連関していること,第4の波で情報科学が貢献,いよいよ抗体医薬が本格化することを強調した(概念図).そこからわずか4年余りで,本書の題目の通り,「治療の可能性が広がる抗体医薬」となりつつある.イノベーションは加速し,本邦からもいよいよ世界を席巻する抗体医薬品が上市されてきている.このような背景のもと,まとめられた本書は,最先端基盤技術,疾患別のバイオロジーと臨床展開の現状,そして,社会実装,の3つの章からなる.以下に,その内容について概説したい.
1.進化・深化を続ける抗体医薬の基盤技術
第1章では,加速する抗体医薬関連の最先端基盤技術についてまとめている.
まず生産である.現在の抗体医薬生産を支えているのは,哺乳動物細胞,特にCHO細胞を用いた組換えタンパク質生産技術である.その歴史的経緯からプラットフォーム化,セルエンジニアリングによるさらなる深化について述べている(1章-1).生産の効率化と低コスト化は医療経済の観点からも大きな課題となり,その技術革新に期待がかかる.
次に,ヒト抗体産生マウス開発についてまとめている(1章-2).初期のハイブリドーマ法により調製された抗体は,当然のことながらマウス抗体となり,ヒトに投与する際には免疫原性の問題が大きくのしかかっていた.その回避のためには,高度な染色体工学技術が要請されるが,世界各国の熾烈な競争のなか,優れたマウスが開発され,いまや,抗体医薬品開発の標準的プラットフォームとなっている.
タンパク質を抗原とする抗体医薬開発では,抗体が創薬標的を介した機能を引き起こすインターフェイス,すなわち抗原側の高次構造であるエピトープに関する知見がきわめて重要である.創薬標的のエピトープこそが抗体医薬のターゲットなのである(1章-3).最近のCOVID-19治療薬に関しても,エピトープの理解が決定的であることを強く示す知見が多く得られている.また,次世代抗体工学として注目されるフォーマットである,二重特異性抗体の開発研究においても,エピトープに基づく設計の重要性が指摘されている.
同時に臨床開発の失敗の原因として,ターゲットバリデーションが不十分であることが認識されつつある.創薬ターゲットの選択には,その候補の多角的なバリデーションが必須である.1章-4では,患者がん移植モデル(PDX)とターゲットバリデーションに関して,薬理学的観点を中心に述べている.ゼブラフィッシュを用いた方法論は,その応用展開が強く期待されるところである.
drug delivery system(DDS)と体内動態の観点が,特にがん治療に関連する次世代抗体医薬品開発では重要である.抗体薬物複合体(antibody-drug conjugate:ADC)とT細胞二重特異性抗体について,1章-5で現状をわかりやすくまとめている.
タンパク質工学という観点での技術革新は,何をおいても二重特異性抗体の開発であろう.中外製薬の井川らが,その成功例を,工業的製法の確立に至るまでの過程を迫力ある記述でまとめている.彼らは,さまざまな工学的アプローチをパネル化できるレベルまでその技術基盤を磨き上げており,国際的にもきわめて高い評価を受けている.患者様に寄り添いつつ,その治療のために技術を洗練させる姿勢は,特筆に値するものである(1章-6, 7).
エフェクター機能に関連するFc領域に関する基礎研究と工学的アプローチの現状と今後については,1章-8でまとめている.構造情報に基づく高機能化,とりわけ糖鎖工学的アプローチに関しては,抗体のエフェクター機能に関する本質を突く優れた研究であり,後述の眞鍋ら(1章-11)の方向性と合わせて,今後の抗体医薬品高機能化の中核をなすイノベーションを導くものである.
がんの薬物療法のフェーズを変え,DDSの概念をとり入れた創薬・治療戦略の開発を加速させているのがADCである.1章-9で臨床的観点を中心にADCについてまとめている.また,関連技術としてその応用範囲の広がりを見せつつあるのが,伊東らが開発しているCCAP法である(1章-10).初期開発品から,最新の進化型についても述べられている.さまざまな分子を複数抗体に結合させ,抗体をデリバリー素子として用いることで,創薬戦略をアップデートさせることが期待されている.さらに,デリバリー素子としての抗体の安全域を広げるものとして調製が試みられてきているのが,糖鎖均一抗体である.1章-11では,糖鎖均一化に関する技術を先鋭化させ,さらに糖鎖部分に薬物を結合させ,均一ADCを作製する手法の開発について解説している.抗体医薬の治療応用が拡大していくなかで,重要な基盤技術になることは想像に難くない.
抗体医薬のフォーマットはIgGにとどまらない.ここでは,IgG以外のフォーマットを応用した抗体について,特に最近進展著しいシングルドメイン抗体(ナノボディ,VHH抗体,VNAR抗体)をとり上げている.1章-12, 13において解説するように,IgGあるいはFab断片に比して,工学的に有利なドメインサイズであることに加え,従来の抗体とは異なる標的結合様式を示すことが明らかになりつつある.人工ライブラリー設計の新たな指針の提案,相互作用機構の詳述に基づく分子設計の提案も含め,今後タンパク質工学的アプローチの進展が大きく期待される.さらに,ペプチド創薬とタンパク質工学を融合する新技術,LassoGraft Technologyについて,1章-14で紹介している.本邦発の独創性の高い技術であることに加え,ペプチド創薬の可能性をさらに高めるという点でも,今後の発展が強く期待されるものである.タンパク質の本質的理解がこの技術を進化・深化させることはいうまでもなく,タンパク質工学の究極の一つである,といってよいだろう.
第1章の終わりには,抗体医薬イノベーションの第4の波の中核となるバイオインフォマティクスについてとり上げた.安定性,結合能に関する分子設計の現状と今後については,1章-15でわかりやすくまとめている.抗体コンピューター設計はAI技術のその先,Beyondにあることがわかり,今後の進展に期待がかかるところである.最近特に注目されているレパトア解析とその応用に関しては,1章-16で現状をわかりやすくまとめている.抗体機能の本質と密接に紐づくレパトア解析の進展が,今後の抗体医薬を決定づけることはいうまでもない.さらに,深層学習については,1章-17で現状と研究例の紹介を通じて,問題点と今後の展開を議論している.イノベーションの第4の波はすでに到来し,大きなうねりになっているのである.
2.拡大を続ける抗体医薬の疾患治療への応用
第2章では,疾患別のバイオロジーとして,進展著しい,拡大しつつある疾患治療応用の実例について,代表的なものを挙げている.
がんでは,糖鎖不全にはじまる糖鎖修飾の異常が治療のための有力な標的とされてきたものの,今まで特異性創出が難しいとされていた糖タンパク質を,現実的開発研究に展開する技術(2章-1),そして,抗PD-1抗体を中心とした免疫チェックポイント阻害剤とその周辺(2章-2),免疫関連有害事象の機序(2章-3)についてまとめている.いずれも抗体医薬のトップランナーとして走り続けているがん治療に関する現状把握と今後に関する議論であり,重要な示唆を与えるものである.
感染症では,COVID-19に対する抗体医薬の開発(2章-4)と,今後大きな課題となる細菌感染症に対する抗体医薬開発の現状(2章-5)についてまとめている.前者では,構造生物学的アプローチと抗体医薬の長所が合致しており,先に述べた,エピトープ構造理解の重要性が最も強調されていることがわかる.多重変異と標的抗原の構造変化,そして抗体開発に必要な指針等,感染症対策に大きな示唆を与える内容である.後者でも,さまざまな課題を包含しつつも課題解決に向けて大きな展開を見せつつあることがわかり,今後に期待がかかる領域である.
さらに,治療の可能性が広がる例として,関節リウマチ・全身性エリテマトーデス(2章-6),骨粗鬆症(2章-7),神経変性疾患(2章-8),潰瘍性大腸炎(2章-9),加齢黄斑変性(2章-10),喘息(2章-11)をとり上げた.いずれも,高い選択特異性と直接毒性の低さに大きな特徴があり,今までの医学研究にパラダイムシフトを促すものであることがわかる.難治性とされてきた各種疾患への適用例が今後さらに増えていくことを強く期待させるものである.
3.抗体医薬の社会実装に向けての課題
第3章では,社会実装に必須となる観点をまとめている.いよいよ治療応用が広がる抗体医薬の周辺で課題として指摘されている,医療経済,レギュラトリーサイエンス,知財をとり上げている.
医療経済の持続性と革新的医薬品を開発支援する産業エコシステムの構築は喫緊の課題である.3章-1は,疾患治療への応用が広がる抗体と医療経済への圧迫,そしてより優れた医薬品開発意欲を萎縮させないためにも産業エコシステム構築が重要である,と読むことができる.
急速に発展している抗体医薬に対するレギュラトリーサイエンスに関しても,基礎・開発研究者が常に意識すべき重要な観点である.3章-2では,その現状と今後をたいへんわかりやすくまとめている.筆者自身も,抗体医薬開発に資する基礎研究,技術開発研究に加え,レギュラトリーサイエンスに貢献する各種分析法について研究を進めてきたが,特に物性研究と生物活性を常にリンクさせるバイオ医薬品開発の重要性を痛感する場面が多かった.
最後に,知財戦略(3章-3)についてまとめている.疾患治療のためのバイオロジー研究は,物質科学的アプローチにより,治療薬という形で社会実装されるものであり,そこには,知財的観点が不断に要請される.3章-3で述べているように,抗体医薬に関連する知財に関する係争も,相当に本質的な内容が含まれており,今後も「知財戦略」を重要な課題としてとり上げていく必要がある.
おわりに─ヒト生命科学研究の社会実装と次世代医療としての抗体医薬
本増刊号を編集していく過程で,イノベーションが駆動している抗体医薬が,いよいよ治療モダリティの重要な要素として不可欠になってきていることを強く認識するようになった.核酸医薬,遺伝子治療,細胞治療等,さまざまな創薬モダリティの進化・深化が今後加速することはいうまでもない.疾患とその標的に関する本質的な理解に基づく,適切なモダリティの選択が重要になる.抗体医薬はそのフロントランナーであり,そして,今後も重要なモダリティに位置づけられると考えられる.最後に,抗体医薬の開発過程における経験は,他のモダリティの社会実装に直結する内容も多いことを強調したい.本増刊号はその意味でも,ヒト生命科学研究の社会実装と次世代医療,という観点で,重要な方向性を包含したものであると考えている.
文献
- 国立医薬品食品衛星研究所生物薬品部(閲覧2022年10月)
- 津本浩平:次世代抗体医薬の衝撃.実験医学,36:1818-1874,2018
著者プロフィール
津本浩平:東京大学大学院工学系研究科バイオエンジニアリング専攻教授,1991年東京大学工学部工業化学科卒(三浦謹一郎教授),博士(工学).東北大学大学院工学研究科,東京大学大学院新領域創成科学研究科を経て,2010年東京大学医科学研究所教授(’13年より兼務),’13年より現職.’21年より東京大学総長特任補佐.’02年日本生化学会奨励賞,’12年日本学術振興会賞等受賞.専門は分子医工学,タンパク質工学,生命物理化学.



