2 高カリウム血症のマネージメント
 はじめに
はじめに
心疾患および腎疾患の予後改善のためにはレニン-アンジオテンシン-アルドステロン(RAA)系を上手く使っていくことが重要です(上手くというのは,できるだけ長く,ACE阻害薬・ARBであればできるだけ高用量で,中断なく使うと言う意味です.MRAは増量した方がいいかははっきりしたデータはありません).
RAA系の使用には高カリウム血症がついて回る問題です,これをどれだけコントロールしてRAA系を継続するか? が内科医の腕の見せどころです.血液透析が本邦でできるようになったのが1960年代,最も古いポリスチレンスルホン酸ナトリウム(ケイキサレート®)が1971年,ポリスチレンスルホン酸カルシウム(カリメート®)の発売が1975年です.昔の教科書のように打つ手がない時代とは違います.洗練されたKコントロールを行っていきましょう.
 本当にRAA系が必要な患者か考えよう
本当にRAA系が必要な患者か考えよう
「§1.高血圧と腎臓」でも説明しましたが,RAA系の恩恵を受けるのは糖尿病,CKD,心筋梗塞後,左室肥大,心不全の既往,心機能低下例の患者となります.逆に言えば,これらに当てはまらない患者像ではRAA系の恩恵は限定的です(血圧を下げる恩恵が大きく,RAA系の上乗せの恩恵は少ない).実臨床を見ていると,RAA系の投与で受ける恩恵が少ない患者には積極的に導入され,多い患者にはきちんと導入されていないことをよく見かけます.これを改善する必要があります.
 偽物の高カリウム血症に注意
偽物の高カリウム血症に注意
高カリウム血症を見つけて慌てて専門医に電話をかけまくる医師がいますが,それより先にするべきことは患者の状態の確認です.
「バイタルサインはいかがですか?」
電話をとったときに,私が最初に聞くのはこちらです.ここで即答できないのであれば,患者と一緒に深呼吸して血圧と脈拍を測りましょう(医師ではなく患者のです).
さて,高カリウム血症で怖いものは徐脈です.ここをチェックしましょう〔心拍数(HR)=50くらいの徐脈は結構ありますので,普段からバイタルサインをカルテに記載しておくのがよいでしょう〕.さすがにHRが30〜40を下回ると,調子の悪い人が多くなります.
実は臨床の現場で高カリウム血症をきたす状況はしばしばあります(図1).直前の食事で果物や野菜を摂取した,採血前にコーヒーなどの嗜好品を飲んだ,採血で駆血帯を巻いている時間が長かったり強かったりした,採血で手間どって何回もシリンジを引いた,採った後の血液を放置して測った場合などが高カリウム血症をきたす要素となります.これらで0.5〜1.0 mEq/L程度は上がります.しかも,K値と臨床症状はパラレルではありません.高カリウム血症のじつに半分が心電図変化を起こさなかったとあります1,2).
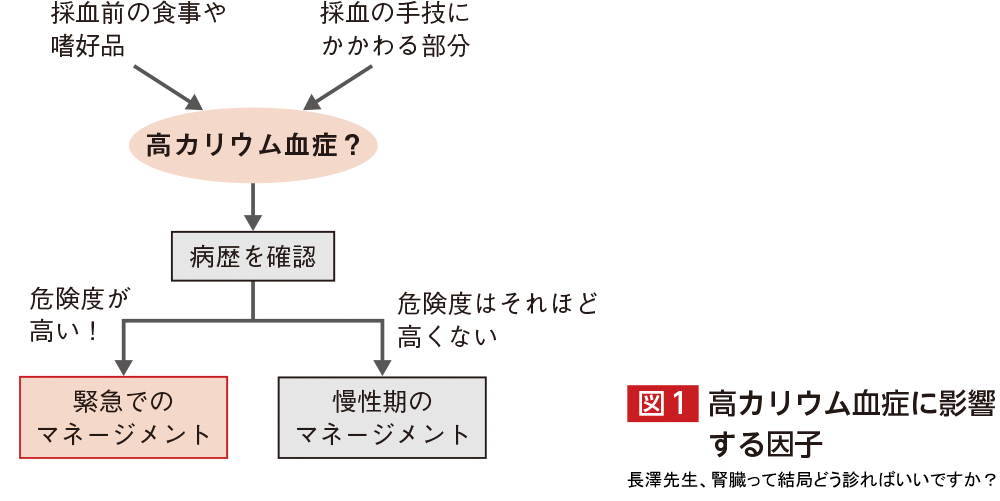
では,どんな病歴に気をつけるべきか? 残念ながら,便利なスコアシステムは見たことがないですが,私の臨床経験やこれまでの論文からは表1の7つが重要です.右側のチェック項目が多いほど危険です.特に夏場で脱水なのに利尿薬を飲んでいる場合などは危険です.
高カリウム血症で一番気にするべきは「今後順調に尿が出ていくか?」です.人間のカリウムの主な排泄は尿からですので,尿が出にくい状況(脱水や心不全)などではかなり注意する必要があります.

 緊急でのマネージメント(図2)
緊急でのマネージメント(図2)
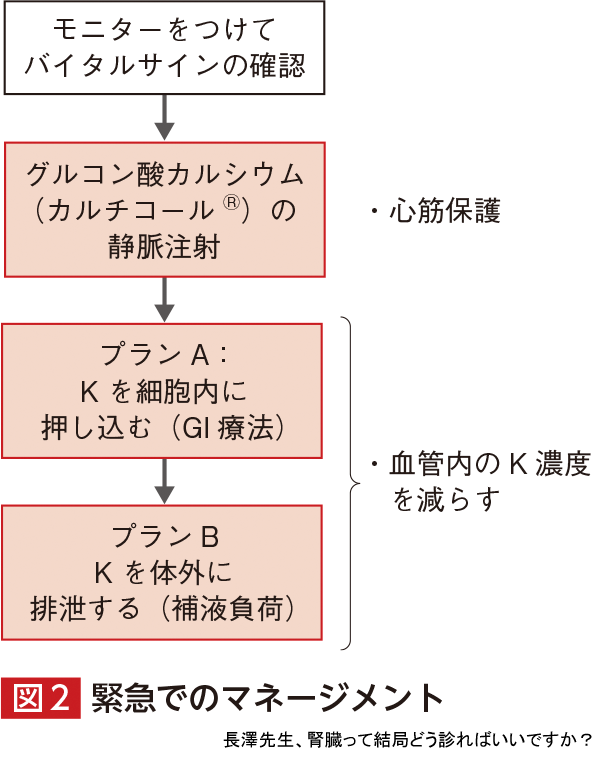
臨床的な症状(徐脈や失神など)がある場合や今後の経過で順調に尿が出ないことを想定する場合には入院での加療を行います.
まず,するべき一手はモニターをつけることです.いつでもバイタルサインが最優先です.
次の一手は高カリウム血症による不整脈を防ぐために,カルチコール®の静脈注射です.
- グルコン酸カルシウム(カルチコール®) 10 mL+生食100 mL(10分程度で)
「3〜4分かけて緩徐に」と言う記載が教科書にありますが,医師や看護師がベッドサイドでつきっきりで注射というのも効率が悪いのですので上記の指示にすることが多いです.注意点があるとすればカルシウム塩などの沈澱や結晶を避けるために単独ラインにした方がよいです(Ca濃度が上がる治療ですので,高カルシウム血症→脱水→AKIなどの病態には使いにくいです.また,身体のなかのKの総量は変わっていないので,あくまで次の治療まで凌ぐための方法です).
続く一手は「血管内のK濃度を減らす」ための手をどれだけ打てるか? になります.血管内にあるKを減らすプランは下記の2つが考えられます.
- プランA:細胞内に押し込む…グルコース-インスリン療法(GI療法),炭酸水素ナトリウムやβ2刺激薬の投与
- プランB:体外に排泄する…利尿をつける,腎代替療法(主に血液透析)
プランAでいかに粘っても,身体のなかのK総量が変わらないためにいずれは限界がきます.よって,プランBで利尿がつくかは常に気にするべきところです(利尿がつかない場合には血液透析をせざるを得ないとなります).
まずはプランAから考えていきましょう.
1)プランA
GI療法の本質は,インスリンによってKを細胞内に押し込む治療です.インスリンの投与により起こりうる低血糖を避けるためにグルコースを入れる治療なので,本質的には「インスリン-グルコース療法」と呼ぶべきだと思いますが,それはさておき,注意点はインスリンはレギュラーインスリンを使うことです(最近の速効型や持続型では不可です).
どのくらいの量を使うかは,絶対的な決まりはないですが私は下記の量で使っています.
- インスリン5単位
+50%グルコース 50 mL
昔の本ではインスリン10単位と書いてあることが多いですが,低血糖の頻度が高いことがわかってきたために,インスリン代謝の落ちているCKDの患者などが多いことを考えると最近はこのくらいの量がトレンドです3,4).実際には体格も考慮する必要があるので
- インスリン0.1単位/kg(max10単位)
+グルコース 25〜50 g
でもよいかもしれません5).
初学者の方は「緩徐に!」と教科書などに書かれてモヤモヤしていると思いますので,実臨床に落とし込むならば下記になるかと思います.
- インスリン5単位〔or 0.1単位/kg(max10単位)〕
+50%グルコース 50 mL ワンショット - インスリン5単位〔or 0.1単位/kg(max10単位)〕
+10%グルコース 500 mL 1時間で
炭酸水素ナトリウムは教科書には書かれていますが,質の高いエビデンスを見たことがありませんので,高カリウム血症の場面では無理に使う必要はないかと思います.β 2刺激薬も頻脈などの副作用を考えると適応外の日本では使う必要はないでしょう.
2)プランB
さて,細胞内にKを押し込んで時間稼ぎができたとして,身体全体のKの総量は変わりません.どうしてもKを外に出す必要があります.利尿をつけるには補液負荷がベストです.
- 生理食塩水 500 mL/時(心機能,腎機能で調整)細胞外液でもOK
この場面では,Kフリーにはこだわる必要がないと思います.すでに高カリウム血症なので4 mEq/L程度の濃度の補液をしても大勢には影響しません(生食を入れることで高Cl性のアシドーシスの懸念はありますが,ここが議論になったことをみたことがありません).
利尿をつけることができれば尿量に応じてKは下がっていきます.
ループ利尿薬はどうするか?
ではループ利尿薬はどうしましょうか? ループ利尿薬は長期的に使用すると低カリウム血症をきたしますが,フロセミド投与でどのくらいK排泄が増えるかというと,これはかなり難しい問題です.K排泄は血清K値やインスリンやアルドステロンなどのホルモンにより大きく影響されていますが,とても古い論文によると24時間でのK排泄が42±19 mEqから95±18 mEqへ増加しています6).ただしこれは浮腫がある患者ですので,恒常性を保とうとして尿の排泄が多くなったと考えています.通常はK排泄の多寡は20 mEq/日やスポット尿で15 mEq/gCreを基準に考えることが多いですが,血清K値が高いのに尿中排泄が低下している,血清K値が低いのに尿中排泄が増加しているのがおかしいと気づけるのが大事です.
人間の身体の中のKの総量は50〜55 mEq/kgであり(70 kgで3,500 mEq),1〜2%程度が細胞外液です.1日の食事などからの摂取量が50〜100 mEqで,尿からの排泄とこれが釣り合うことにより,K値は一定になると考えられています.(腸管からの排泄は通常は尿の10%程度だといわれており,腎機能障害がすすむと便中K排泄が3〜4倍まで増えるという話はあります)7〜12).
いろいろと書きましたが,要は「尿量が十分に確保できることが,高カリウム血症の治療の最重要ポイントである」となります.そのために,十分な補液がまず大事で,体液量過剰になった際には下記のようにフロセミドで上乗せをするという捉え方になります.
- フロセミド 20〜200 mg 静脈注射(体液量過剰のとき,腎機能に合わせて適宜増.脱水のときは禁忌)
一生懸命ケイキサレートを注腸する意味も少ないと考えています(浣腸などの直腸への投与でのトラブルや医療事故は意外と多いです).
補液とフロセミドの静脈注射をして30分〜1時間ですみやかに尿が確保できない(具体的には,1 mL/kg/時程度が確保できない)場合には,腎代替療法に移行することを検討しましょう.
急性期のK吸着薬として
- ジルコニウムシクロケイ酸ナトリウム水和物(ロケルマ®) 1回10 g,1日 3回,2日以後は1回5 g,1日1回
を入れておくのもよいかと思います(経口摂取できない場面ではどのくらい有効かはわかりませんが,消化管内にあるKを吸着してくれる可能性があると思います).
 慢性期のマネージメント(図3)
慢性期のマネージメント(図3)

さて,入院中のK管理は前述のようになりますが,じつは入院中は結構ラクです.モニターをつけて,頻回に採血ができて,尿量も測定できるからです.一方,外来は月1回だとすると結構気を遣います.
「§1.高血圧と腎臓」で薬の選び方は話しましたが,RAA系導入のポイントは下記になります.
 RAA系導入のポイント
RAA系導入のポイント
- 添付文書記載量の1/4量から開始
- 開始後2週間でK,Crをチェック
- 夏場の増量は避けつつ,ACE阻害薬,ARBは最大量をめざす(MRAは増やすほど上乗せ効果があるかは不明)
- 患者指導:血圧が低いときはRAA系をスキップ(具体的には収縮期血圧<110 mmHgはスキップと薬袋に書く),ご飯を食べられないときもスキップ
Crは10%上がったら,RAA系薬剤の減量か専門医に相談となりますが,Kはどうでしょう? 非専門医であれば,5.5〜5.9 mEq/Lくらいまでは粘ってほしいと思っております.前述の偽性高カリウム血症がたくさんあるからです.表1のチェックリストを使って危なそうな患者に目を光らせておいて,血圧,体重などをきちんとフォローしてください.
1)K吸着薬
さて,RAA系を導入して高カリウム血症になったときには,
- KのINを減らすか?
- KのOUTを増やすか?
いずれかの戦略をとります.INを減らす作戦としては「K吸着薬」となります.じつは最近の流れとしては,CKDでも果物や野菜が健康上重要であることが示唆されております13).これらを制限してもKに対してのインパクトが薄いという話があるくらいです14).このあたりは「§4.CKDの食事指導」で解説します.
ロケルマ®を使った報告では,保存期のCKDでは野菜果物の制限なしにKを良好にコントロールすることができたとあります15).
となると,私の一手は
- ジルコニウムシクロケイ酸ナトリウム水和物(ロケルマ®) 1回5 g,1日1回
となります.この論文を見たとき「本当か!?」と思ったのですが,実臨床で使ってみると私としては理想的にKをコントロールすることができております.この薬を推すと「高い」と言われますが,高カリウム血症による入院は外来で診た場合と比べて5倍は医療費が高いです16).
しかも,今後病院の統廃合が進み,軽症の場合には入院できない時代がやってくると読んでおりますので,このコストをよく考えていただきたいと思います.
当然,診療単価が安い病床というのはあるので,その場合には他のK吸着薬を使うことになりますが,下記のようになります.
- ケイキサレート®散 1日30 g,2回〜3回に分けて投与
- ケイキサレート®ドライシロップ 1日30 g,2回〜3回に分けて投与
- カリメート®散 1日15〜30 g,2回〜3回に分けて投与
- カリメート®ドライシロップ 1日15〜30 g,2回〜3回に分けて投与
- カリメート®経口液 1日15〜30 g,2回〜3回に分けて投与
- アーガメイト®ゼリー 1日3〜6個(75〜150 g),2〜3回に分けて投与
これらの薬を使うときには,「腹部手術の既往」や「イレウスの既往」には十分に注意してください.腸管内で膨張するためにトラブルが多いです.そのような既往がある場合にはロケルマ®が圧倒的に使いやすいです.
もう一点考えておくことはアドヒアランスです.じつはロケルマ®は慢性期には1日1回の内服です.既存薬が1日に2〜3回投与であることに比べてきちんと飲めます.経験上アドヒアランスが悪い人ほどロケルマ®が効く印象です.逆にアドヒアランスがよい場合にはこれまでの薬でもよいだろうとなります.
2)利尿薬
慢性期に利尿薬をどうするか? も結論の出ていない問題です.サイアザイド系薬剤もループ利尿薬も,漫然と使うと低カリウム血症をきたします.サイアザイドは降圧薬として前項で説明したので,ループ利尿薬について話しておきます.
まず,急性心不全に対してループ利尿薬で有効性があるという報告は結構ありますが17〜19),長期予後が改善したという報告は限定的です.むしろ,ループ利尿薬を使うと予後が悪いという報告が多いです20,21).ただし急性期を乗り切らずに慢性期に移行することはできないので簡単に良いか悪いかは判断できません.
短時間作用のフロセミドは急速な利尿による交感神経の活性化やリバウンドでの再吸収をきたすと言われており,作用時間が長いアゾセミドは,フロセミドより長期予後がよい,という報告もあります22,23).トラセミドも同様の報告があります.こちらには抗アルドステロン作用があると言われております24).個人的には利尿薬のオマケの抗アルドステロン効果を期待するのであれば,MRAを入れた方がよいと思います.
さて,利尿薬自体が悪いというよりは,利尿薬を使わないと管理できない病態あるいは生活習慣が問題な気もしますが,使わずにすむには越したことがないです.となると,利尿薬ですので体液量過剰のときに使うという使い方がベストになります.基準体重を決めて,○○kgを超えたときに内服という使い方が便利です.
- フロセミド 1回20〜200 mg,1日1回(基準体重を超えたとき)
- アゾセミド 1回30〜60 mg,1日1回(基準体重を超えたとき)
- トラセミド 1回4〜8 mg,1日1回(基準体重を超えたとき)
フロセミドはバイオアベイラビリティーに個人差があるために,効かない場合は増量を考える必要があるでしょう.
またアシドーシスも高カリウム血症のリスクになるのでマネージメントした方がよいですが14),これは「§5.血糖と腎臓」で解説しましょう.
 まとめ
まとめ
- 心疾患および腎疾患の予後改善のためにはRAA系を上手く使うことが重要
- RAA系の使用には高カリウム血症がつきもの
- 高カリウム血症の緊急のマネージメントでは,バイタルサインをモニタリングしながらカルチコール®静注し,次に血管内のK濃度を減らし,その後体のKの総量を減らす
- 高カリウム血症の慢性期のマネージメントでは,K吸着薬や利尿薬を用いる
文献
- Acker CG, et al:Hyperkalemia in hospitalized patients: causes, adequacy of treatment, and results of an attempt to improve physician compliance with published therapy guidelines. Arch Intern Med, 158:917-924, 1998(PMID:9570179)
- Montague BT, et al:Retrospective review of the frequency of ECG changes in hyperkalemia. Clin J Am Soc Nephrol, 3:324-330, 2008(PMID:18235147)
- McNicholas BA, et al:Treatment of Hyperkalemia With a Low-Dose Insulin Protocol Is Effective and Results in Reduced Hypoglycemia. Kidney Int Rep, 3:328-336, 2018(PMID:29725636)
- Clase CM, et al:Potassium homeostasis and management of dyskalemia in kidney diseases: conclusions from a Kidney Disease: Improving Global Outcomes (KDIGO) Controversies Conference. Kidney Int, 97:42-61, 2020(PMID:31706619)
- Moussavi K, et al:Management of Hyperkalemia With Insulin and Glucose: Pearls for the Emergency Clinician. J Emerg Med, 57:36-42, 2019(PMID:31084947)
- Alexander WD, et al:The urinary sodium: potassium ratio and response to diuretics in resistant oedema. Postgrad Med J, 53:117-121, 1977(PMID:323834)
- Hayes CP Jr, et al:An extravenal mechanism for the maintenance of potassium balance in severe chronic renal failure. Trans Assoc Am Physicians, 80:207-216, 1967(PMID:6082243)
- Sandle GI, et al:Enhanced rectal potassium secretion in chronic renal insufficiency: evidence for large intestinal potassium adaptation in man. Clin Sci (Lond), 71:393-401, 1986(PMID:3757437)
- Panese S, et al:Mechanism of enhanced transcellular potassium-secretion in man with chronic renal failure. Kidney Int, 31:1377-1382, 1987(PMID:3613409)
- Sandle GI, et al:Evidence for large intestinal control of potassium homoeostasis in uraemic patients undergoing long-term dialysis. Clin Sci (Lond), 73:247-252, 1987(PMID:3652631)
- Mathialahan T & Sandle GI:Dietary potassium and laxatives as regulators of colonic potassium secretion in end-stage renal disease. Nephrol Dial Transplant, 18:341-347, 2003(PMID:12543890)
- Sumida K, et al:Laxative Use and Risk of Dyskalemia in Patients with Advanced CKD Transitioning to Dialysis. J Am Soc Nephrol:doi:10.1681/ASN.2020081120, 2021(PMID:33547216)
- Sussman EJ, et al:Let Them Eat Healthy: Can Emerging Potassium Binders Help Overcome Dietary Potassium Restrictions in Chronic Kidney Disease? J Ren Nutr, 30:475-483, 2020(PMID:32147285)
- Ramos CI, et al:Does dietary potassium intake associate with hyperkalemia in patients with chronic kidney disease? Nephrol Dial Transplant, 36:2049-2057, 2021(PMID:33247727)
- Sussman EJ, et al:Let Them Eat Healthy: Can Emerging Potassium Binders Help Overcome Dietary Potassium Restrictions in Chronic Kidney Disease? J Ren Nutr, 30:475-483, 2020(PMID:32147285)
- Kanda E, et al:Clinical and Economic Burden of Hyperkalemia: A Nationwide Hospital-Based Cohort Study in Japan. Kidney Med, 2:742-752.e1, 2020(PMID:33319198)
- Matsue Y, et al:Time-to-Furosemide Treatment and Mortality in Patients Hospitalized With Acute Heart Failure. J Am Coll Cardiol, 69:3042-3051, 2017(PMID:28641794)
- He X, et al:Effect of aggressive diuresis in acute heart failure with reduced and preserved ejection fraction. ESC Heart Fail, 8:3248-3256, 2021(PMID:34076960)
- Faselis C, et al:Loop Diuretic Prescription and Long-Term Outcomes in Heart Failure: Association Modification by Congestion. Am J Med, 134:797-804, 2021(PMID:33359271)
- Eshaghian S, et al:Relation of loop diuretic dose to mortality in advanced heart failure. Am J Cardiol, 97:1759-1764, 2006(PMID:16765130)
- Ahmed A, et al:Heart failure, chronic diuretic use, and increase in mortality and hospitalization: an observational study using propensity score methods. Eur Heart J, 27:1431-1439, 2006(PMID:16709595)
- Masuyama T, et al:Superiority of long-acting to short-acting loop diuretics in the treatment of congestive heart failure. Circ J, 76:833-842, 2012(PMID:22451450)
- Kasama S, et al:Comparative effects of long and short-acting loop diuretics on mortality in patients with chronic heart failure. Int J Cardiol, 244:242-244, 2017(PMID:28645802)
- Cosín J & Díez J:Torasemide in chronic heart failure: results of the TORIC study. Eur J Heart Fail, 4:507-513, 2002(PMID:12167392)



