概論
COVID-19 その重症化と後遺症を乗り越えるために
Overcoming severe COVID-19 and long COVID
熊ノ郷 淳
Atsushi Kumanogoh:Department of Respiratory Medicine and Clinical
Immunology, Graduate School of Medicine, Osaka
University(大阪大学大学院医学系研究科呼吸器・免疫内科学)
COVID-19パンデミックから3年が経過したが,いまだにCOVID-19は社会的活動に大きな影響を与えている.mRNAワクチンの普及とウイルス自身の変異(オミクロン株の流行)により,その重症化率は下がったが,2022年12月時点で感染者数自体は増加傾向にあり,関連死者数も増加している.さらに,COVID-19罹患後も一部の患者では後遺症に長く苦しむこととなり,ポストコロナ時代にはこれらが課題となっている.本特集ではこれまでに明らかになった免疫学的知見について整理することで,これらの課題について解決の糸口となることを願う.
はじめに
COVID-19が武漢から全世界に広がり3年が経過したが2022年12月現在,ワクチンが普及した日本においても第8波がおとずれ感染者数は増加の一途をたどっている(https://covid19.who.int/region/wpro/country/jp).また,一度は収束したかにみえた中国などの諸外国においても感染者数が増加に転じている地域もあり,COVID-19の猛威はいまだに収束してはいない.ワクチンの普及やウイルスの変異などにより重症化率は下がったが,感染者数自体は増加しており,重症化のメカニズムのみならず後遺症のメカニズムを解明することが今後のポストコロナ時代を乗り切るために必要である.
本特集ではCOVID-19研究の最前線で活躍されている研究者の先生方に,COVID-19の重症化,およびCOVID-19後遺症(いわゆるlong COVID)について,それぞれが専門とする領域の視点からの解説をお願いした.まず,感染の自然史と疫学について,忽那先生(忽那氏の稿)に解説をお願いした.重症化の遺伝的背景については福永先生(南宮氏らの稿)に,COVID-19の重症化で世間一般の注目を集めたウイルス感染時の免疫応答に関して,B細胞に注目した解説を高橋先生(安達氏らの稿)に,T細胞に注目した解説を山﨑先生(坂井氏らの稿)にお願いし,自然免疫に関してはわれわれが執筆した(網屋氏らの稿).さらに,重症化・後遺症リスクとかかわる性差に注目した免疫応答について上野先生(上野氏の稿)に,パンデミック当初から重症化リスクとしてよく知られている肥満と関連した内分泌・代謝とのかかわりについては下村先生(シン氏らの稿)にお願いした.また,多くの人々の関心を集めている変異株などのウイルス要因については河岡先生(浦木氏らの稿)に解説をお願いした.
1COVID-19の重症化メカニズム
当初よりCOVID-19の重症化メカニズムとして注目されていたのが,免疫の暴走とも言われるサイトカインストームの存在である1)2).サイトカインストームはCAR-T細胞療法による腫瘍崩壊時や成人Still病などの膠原病患者の一部に発症することは以前から知られていたが,COVID-19パンデミックにより,サイトカインストームという用語がより多くの人に知られるようになった.サイトカインストームとは何らかの原因により暴走した免疫が,サイトカインを過剰産生し生命を脅かしてしまう状態である3)と考えられ,実際に中等症Ⅱ〜重症COVID-19に対する薬物療法として,ステロイド,IL-6受容体阻害薬であるトシリズマブあるいはJAK阻害薬であるバリシチニブによる免疫抑制療法が,抗ウイルス薬のレムデシビル投与とともに行われている(図1).

一部の患者でなぜサイトカインストームが生じるのか,その理由についてはいまだ十分に解明されているとは言えない.しかし,その原因の一端として,抗ウイルス作用の中心的サイトカインであり,自然免疫系の細胞が主に産生するⅠ型IFNおよびⅢ型IFN応答不全が関与している可能性が指摘されている4).Ⅰ型IFN応答が不十分になってしまう理由の一つに,先天的にⅠ型IFN応答に重要な遺伝子の異常がある可能性があり,COVID-19重症者の遺伝学的アプローチで13の遺伝子にloss of functionの可能性がある変異が濃縮されていることが報告されている5).また,同様にⅠ型IFNの産生に重要な分子であるDOCK2の機能低下が重症化に寄与している可能性がわが国の「コロナ制圧タスクフォース」の成果として報告されている(南宮氏らの稿).また,遺伝的要因以外にも,抗Ⅰ型IFN抗体の存在がSARS-CoV-2感染時のIFN応答を減弱してしまい,重症化の要因になっている可能性も報告されている6).われわれの研究でも,COVID-19罹患者の中でも,呼吸不全であるARDS合併例ではARDS非合併例と比較して,末梢血単球のⅠ型IFN誘導遺伝子が低下していることが確認されている7).SARS-CoV-2感染時の生体防御のもう一つの要である獲得免疫系に関するメカニズムについては,シングルセル解析技術の手法を用いたT細胞のクローンレベルでの解析の説明を山﨑先生に,液性免疫に注目した抗体の働き・進化についての詳細な説明を高橋先生にお願いしており,そちらを参照されたい(坂井氏らの稿,安達氏らの稿).また,パンデミック当初から肥満・高齢はCOVID-19重症化のリスクファクターとして広く知られていたが,その理由はわかっていなかった.下村先生らは肥満や高齢者の脂肪組織で高発現しているシャペロンタンパク質のGRP78がCOVID-19の病態とかかわっていることを報告しており(シン氏らの稿),これらのリスクファクターとCOVID-19の重症化を結びつけるメカニズムの一つと考えられる.
重症化予防の戦略として最も重要なものの一つであるワクチン開発については,mRNAワクチンが劇的な予防効果をもたらし,継続的な接種が励行されている.しかしながら,ワクチンによる免疫がいつまで維持されるのか,ワクチンをいつまでくり返し接種すべきなのかについてはいまだに答えが出ていない.接種時に免疫応答の指標としてよく用いられている中和抗体の産生だけに注目してみても,くり返すワクチン摂取による抗体の進化について,メリットとデメリットが指摘されている(安達氏らの稿).自然免疫に注目してみると,2回目のワクチン接種時に単球のエピゲノム変化を伴ったⅠ型IFN応答の亢進が観察されることをわれわれは見出しているが,この現象が一過性であることもわかっており,今後のくり返す接種による変化についてさらなる解析が必要である(網屋氏らの稿).また,ウイルス自身の変化についても忘れてはならず,SARS-CoV-2は免疫機構をすり抜けるために自身も変化し続けており(浦木氏らの稿),宿主側の免疫応答の解明とともに,ウイルス側の変化が免疫応答に与える影響についても明らかにしていくことが今後のCOVID-19克服には必要である.
2COVID-19後遺症
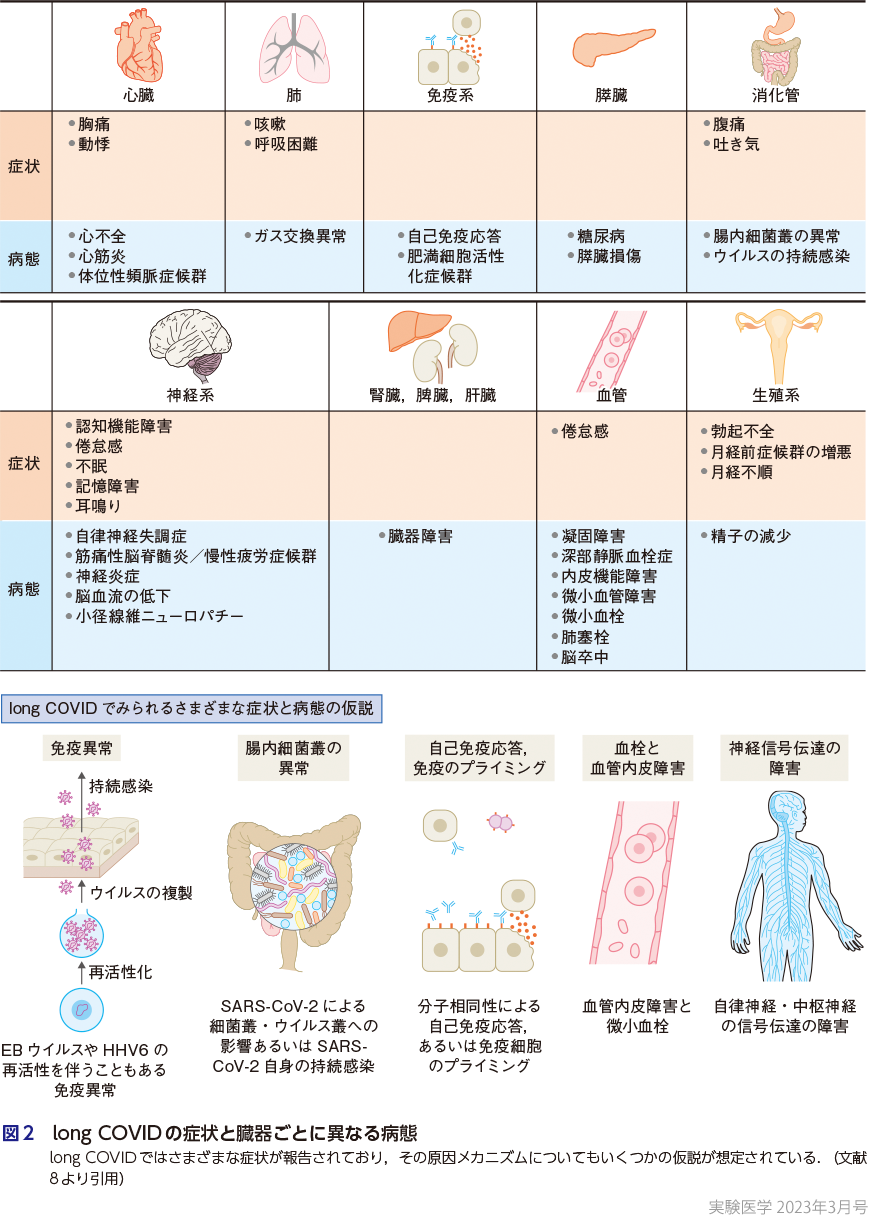
COVID-19に罹患した後に,一部の患者でlong COVIDあるいはpost-acute sequelae of COVID-19,post COVID-19 condition 等と言われる後遺症が生じることが報告されている.long COVIDの明確な定義はないが,その多くは急性期症状や経過中に新たに生じた症状などが長期にわたり持続し,ほかの疾患で説明できない状態をさし,疲労感・倦怠感,関節痛,筋肉痛などの症状が報告されている(図2)8)9).long COVIDには重症化のメカニズムと同様に,自然免疫,獲得免疫のいずれの免疫応答がかかわっていると考えられているが,それ以外にも神経の信号伝達異常などのさまざまな機序が想定されている.さらに,男女差やウイルス側の因子もあり,特に,重症化とは対照的に女性の方がリスクが高いと報告されており,そのメカニズムの解明が注目される(上野氏の稿).
おわりに
COVID-19パンデミックから3年が経過し,社会の風景は様変わりしたが最新の研究によりCOVID-19重症化,後遺症のメカニズムについて徐々に明らかとなってきた.また,社会的にもCOVID-19の感染症法上の位置付けを現在の2類相当から5類に変更することが検討されており,ポストコロナ時代へ大きく動こうとしている.COVID-19パンデミックがもたらしたさまざまな教訓・知見を糧にした免疫学の発展が,ポストコロナ時代を乗り切り,今後まだ見ぬ新規感染症への対策ともなることを願う.
文献
- Fajgenbaum DC & June CH:N Engl J Med, 383:2255-2273, doi:10.1056/NEJMra2026131(2020)
- Montazersaheb S, et al:Virol J, 19:92, doi:10.1186/s12985-022-01814-1(2022)
- McGonagle D, et al:Nat Rev Rheumatol, 17:145-157, doi:10.1038/s41584-020-00571-1(2021)
- Lamers MM & Haagmans BL:Nat Rev Microbiol, 20:270-284, doi:10.1038/s41579-022-00713-0(2022)
- Zhang Q, et al:Science, 370:eabd4570, doi:10.1126/science.abd4570(2020)
- Bastard P, et al:Science, 370:eabd4585, doi:10.1126/science.abd4585(2020)
- Yamaguchi Y, et al:JCI Insight, 7:e163347, doi:10.1172/jci.insight.163347(2022)
- Davis HE, et al:Nat Rev Microbiol:1-14, doi:10.1038/s41579-022-00846-2(2023)
- 厚生労働省:COVID-19診療の手引き 別冊 罹患後症状のマネジメント.
- 厚生労働省:COVID-19診療の手引き 第8.1版.
本記事のDOI:10.18958/7195-00001-0000422-00
著者プロフィール
熊ノ郷 淳:1991年大阪大学医学部卒業.2年間の臨床経験ののち,大阪大学大学院医学系研究科にて岸本忠三教授に師事する.’97年から大阪大学微生物病研究所分子免疫制御分野(菊谷仁教授)に移り,それまで神経ガイダンス因子とされていたセマフォリン分子の免疫系における役割を世界ではじめて明らかにした.2006年から大阪大学免疫学フロンティア研究センター(IFReC)教授,’11年から大阪大学大学院医学系研究科呼吸器・免疫内科学教授,’21年から大阪大学医学部長を務め,臨床と基礎の橋渡しとなるトランスレーショナルリサーチを実践している.